Содержание:
- 1 Синдром гипоплазии левых отделов сердца
- 1.1 Электронная версия книги изданная НЦССХ им. Бакулева. Авторы С. М. Крупянко, Г. Э. Фальковский Сердце ребёнка Технический раздел
- 1.2 Синдром гипоплазии левых отделов сердца
- 1.3 Синдром гипоплазии левых отделов сердца
- 1.4 Причины и морфология синдрома гипоплазии левых отделов сердца
- 1.5 Особенности гемодинамики при синдроме гипоплазии левых отделов сердца
- 1.6 Симптомы синдрома гипоплазии левых отделов сердца
- 1.7 Диагностика синдрома гипоплазии левых отделов сердца
- 1.8 Лечение синдрома гипоплазии левых отделов сердца
- 1.9 Прогноз синдрома гипоплазии левых отделов сердца
- 1.10 Сглос синдром гипоплазии левых отделов сердца
- 1.11 ПАТОФИЗИОЛОГИЯ
- 1.12 ДИАГНОСТИКА
- 1.13 ЛЕЧЕНИЕ И НАБЛЮДЕНИЕ
Синдром гипоплазии левых отделов сердца
Электронная версия книги изданная НЦССХ им. Бакулева. Авторы С. М. Крупянко, Г. Э. Фальковский Сердце ребёнка Технический раздел
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.
[center]Г. Э. Фальковский, С. М. Крупянко [url=https://forum. dearheart. ru.

Форум родителей детей и взрослых с врождённым пороком сердца » Технический раздел » Сердце ребёнка » Синдром гипоплазии левых отделов сердца

Еще совсем недавно этот порок был абсолютно смертельным. Ребенок погибал в течение первой недели жизни, и никакой хирургической помощи ему оказать было невозможно.
Сегодня дело обстоит иначе и, если все сделано вовремя и правильно, то есть хорошие шансы его спасти. Именно – спасти, т. к. сразу после рождения время его жизни отсчитывает не месяцы и дни – а часы, и даже минуты.
Слово «гипоплазия» означает «уменьшение в размерах». При этом пороке левый желудочек, т. е. главный, основной – почти полностью не развился. Но мало этого. Вместе с ним не развился ни вход в него, т. е. митральный клапан, ни выход из него – т. е. участок восходящей аорты вместе с ее клапаном. Вместо аорты имеется небольшой сосудик диаметром 1 — 3 миллиметра, по которому кровь поступает в коронарные артерии, а участка восходящей аорты – нет.
Огромный правый желудочек, получающий кровь из правого предсердия и левого предсердия через дефект в межпредсердной перегородке, нагнетает всю кровь в легочную артерию и легкие. Часть ее через отрытый артериальный проток поступает в большой круг, но только малая часть. Жизнь, таким образом, зависит от наличия двух сообщений – межпредсердного и межартериального, которые, во-первых, недостаточны, а во-вторых, сразу после рождения могут закрыться, как это бывает в норме. Иначе, как гемодинамической катастрофой это назвать нельзя, и без самых экстренных мер ребенок погибнет.
Диагноз может быть установлен еще внутриутробно, и это – чрезвычайно важный момент, когда и родители, и врачи должны взвесить все имеющиеся возможности для оказания немедленной помощи. Важна тут не только подготовка к немедленным действиям, но и абсолютная решимость пройти с ребенком весь трудный поэтапный путь его дальнейшего лечения, который займет несколько первых лет его жизни.
Каждый из этих этапов для ребенка может оказаться последним, так как все они связаны с огромным риском. Но всегда, даже если это слабое утешение, надо помнить, что и вы, и врачи сделали все сегодня возможное, чтобы его спасти.
Первую операцию выполняют в первые дни жизни. Подходы к первому этапу хирургической коррекции могут быть различными и зависят от клиники, мастерства хирурга, готовность кардиохирургического стационара к выхаживанию и ведению этой экстремально сложной категории пациентов. Это может быть и операция с искусственным кровообращением, иногда – достаточно длительного, т. к. нужно сделать полную реконструкцию резко суженной восходящей аорты. Это достигается вшиванием эластичного биологического протеза такой формы, что в результате легочная артерия и аорта становятся единственным сосудом, отходящим от правого (единственного) желудочка. Чтобы обеспечить достаточное смешение крови, создают большой дефект межпредсердной перегородки, а кровоток в легкие направляют через артерио-легочный анастомоз. Как можно видеть из этого описания, это очень большая и сложная операция, которую можно делать исключительно в центрах, имеющих большой опыт операций на сердце у новорожденных детей.
Но даже в самых крупных и известных во всем мире учреждениях США смертность после этого этапа достигает 20 – 40 процентов.
Мы приводим эти цифры, чтобы подчеркнуть, что при синдроме гипоплазии левых отделов сердца хирургия – это единственный возможный, но далеко не безопасный путь. Но, поскольку мы говорим о спасении жизни, то даже сами попытки всегда оправданы.
В последние годы в нескольких клиниках мира внедрен метод, выживаемость после которого близка к 90% — так называемая гибридная операция стентирования открытого артериального протока и двустороннего раздельного суживания легочных артерий.
В клиниках, имеющих большой опыт подобных операций, второй и третий этапы значительно менее рискованны, чем первый – наиболее трудный. Ребенку предстоит жизнь с одним желудочком и все, сказанное выше о пороках, для которых операция Фонтена является заключительным этапом хирургического лечения, относится в полной мере и к этому пороку.
Еще 10 – 15 лет назад дети с синдромом гипоплазии левых отделов сердца не подлежали операции вообще. А ведь синдром – один из пяти наиболее часто встречающихся врожденных пороков сердца. Сегодня помощь этим детям возможна, хотя и не всегда. Но, если вы и ваши кардиологи это знают, то надо действовать. И пусть «надежды маленький оркестрик под управлением любви» никогда не оставляет вас на этом трудном пути.
Синдром гипоплазии левых отделов сердца
Синдром гипоплазии левых отделов сердца – группа морфологически близких дефектов сердца, включающих недоразвитие его левых отделов, атрезию или стеноз аортального и/или митрального клапанного отверстия, резкую гипоплазию восходящей аорты или комбинацию этих дефектов. Проявления синдрома развиваются по мере закрытия артериального протока, в первые сутки жизни новорожденного и характеризуются признаками кардиогенного шока: тахипноэ, одышкой, слабым пульсом, бледностью и цианозом, гипотермией. Диагноз синдрома гипоплазии левых отделов сердца можно предположить на основании двухмерной эхокардиографии, катетеризации сердца, рентгенографии, ЭКГ. Ведение больных с синдромом гипоплазии левых отделов сердца предполагает инфузию простагландина Е1; проведение ИВЛ, коррекцию метаболического ацидоза; поэтапную хирургическую коррекцию порока (операция Норвуда — операция Гленна или Геми-Фонтена – операция Фонтена).
Синдром гипоплазии левых отделов сердца
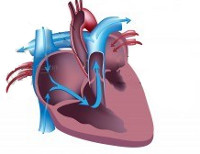
Синдром гипоплазии левых отделов сердца (СГЛОС) – термин, используемый для обозначения критического врожденного порока сердца, характеризующегося резким недоразвитием его левых камер и восходящей части аорты, а также митральным или аортальным стенозом. Синдром гипоплазии левых отделов сердца входит в пятерку наиболее часто встречающихся в кардиологии ВПС, наряду с дефектом межжелудочковой перегородки, транспозицией магистральных сосудов, тетрадой Фалло и коарктацией аорты. СГЛОС составляет 2-4% от всех встречающихся врожденных аномалий сердца, являясь ведущей причиной гибели новорожденных в первые дни и недели жизни. Мальчики страдают данным сочетанным пороком сердца в 2 раза чаще, чем девочки.
Причины и морфология синдрома гипоплазии левых отделов сердца
Причины гипоплазии левых отделов сердца достоверно неясны. Предполагается возможность аутосомно-рецессивного, аутосомно-доминантного и полигенного типов наследования. Наиболее вероятной является теория мультифакториальной этиологии порока.
Различают два морфологических варианта СГЛОС. Первый (наиболее тяжелый) вариант включает гипоплазию левого желудочка и атрезию устья аорты, которые могут сочетаться с атрезией либо стенозом митрального отверстия; при этом полость левого желудочка щелевидна, ее объем составляет не более 1 мл. При втором (наиболее распространенном) варианте порока имеет место гипоплазия левого желудочка, стеноз устья аорты и гипоплазия ее восходящего отдела в сочетании с митральным стенозом; объем полости левого желудочка равен 1-4,5 мл.
Оба варианта гипоплазия левых отделов сердца сопровождаются наличием широкого открытого артериального протока и открытого овального окна, расширением правых отделов сердца и ствола легочной артерии, гипертрофией миокарда правого желудочка; нередко — фиброэластозом эндокарда.
Особенности гемодинамики при синдроме гипоплазии левых отделов сердца
Тяжелые расстройства кровообращения при гипоплазии левых отделов сердца развиваются вскоре после рождения и характеризуются в литературе как «гемодинамическая катастрофа». Сущность нарушения гемодинамики определяется тем фактом, что кровь из левого предсердия не может поступить в гипоплазированный левый желудочек, а вместо этого попадает через открытое овальное окно в правые отделы сердца, где происходит ее смешение с венозной кровью. Эта особенность приводит к объемной перегрузке правых отделов сердца и их дилатации, которые наблюдаются с момента рождения.
В дальнейшем основной объем смешанной крови из правого желудочка поступает в легочную артерию, остальная же часть недонасыщенной кислородом крови через открытый артериальный проток устремляется в аорту и большой круг кровообращения. Ретроградным путем небольшое количество крови поступает в гипоплазированную часть восходящей аорты и венечные сосуды.
Фактически правый желудочек берет на себя двойную функцию, перекачивая кровь в легочный и системный круг кровообращения. Попадание крови в большой круг кровообращения возможно только по артериальному протоку, в связи с чем гипоплазия левых отделов сердца рассматривается как порок с дуктус-зависимым кровообращением. Прогноз для жизни ребенка зависит от сохранения артериального протока открытым.
Тяжелейшие расстройства гемодинамики приводят к выраженной легочной гипертензии вследствие высокого давления в системе сосудов малого круга; артериальной гипотонии, обусловленной неадекватным наполнением большого круга; артериальной гипоксемии, связанной со смешением крови в правом желудочке.
Симптомы синдрома гипоплазии левых отделов сердца
Клинические признаки, указывающие на гипоплазию левых отделов сердца, проявляются в первые часы или сутки после рождения. По своим проявлениям они схожи с респираторным дистресс-синдромом или кардиогенным шоком.
Как правило, дети с СГЛОС рождаются доношенными. У новорожденных наблюдается адинамия, сероватый цвет кожных покровов, тахипноэ, тахикардия, гипотермия. При рождении цианоз выражен незначительно, однако вскоре нарастает и становится диффузным либо дифференцированным, только на нижней половине туловища. Конечности наощупь холодные, периферическая пульсация на них ослаблена.
С первых дней жизни нарастает сердечная недостаточность с застойными хрипами в легких, увеличением печени, периферическими отеками. Характерно развитие метаболического ацидоза, олигурии и анурии. Нарушение системной циркуляции сопровождается неадекватной церебральной и коронарной перфузией, что приводит к развитию ишемии головного мозга и миокарда. В случае закрытия артериального протока ребенок быстро погибает.
Диагностика синдрома гипоплазии левых отделов сердца
Во многих случаях диагноз синдрома гипоплазии левых отделов сердца ставится еще до рождения ребенка при проведении ЭхоКГ плода. При объективном обследовании новорожденного ребенка определяется слабый пульс на руках и ногах, одышка в покое, усиленный сердечный толчок и видимая эпигастральная пульсация; выслушивается систолический шум изгнания, ритм галопа и одинарный II тон.
На ЭКГ отмечается отклонение ЭОС вправо, признаки резкой гипертрофии правых отделов сердца и левого предсердия. Фонокардиография фиксирует наличие низко — или среднеамплитудного систолического шума. Рентгенография грудной клетки при синдроме гипоплазии левых отделов сердца выявляет высокую степень кардиомегалии, шарообразные контуры сердечной тени, усиление легочного рисунка.
Эхокардиография обнаруживает следующие характерные признаки гипоплазии сердца: стеноз устья аорты и ее восходящего отдела, уменьшение размеров левого желудочка и увеличение правого желудочка, грубые изменения митрального клапана.
Зондирование полостей сердца обнаруживает пониженное насыщение крови кислородом в периферических артериях, лево-правый сброс крови на уровне предсердий, повышенное давление в правом желудочке и легочной артерии. Ангиокардиография позволяет визуализировать открытый артериальный проток, гипоплазированную восходящую аорту, резко дилатированный правый желудочек, расширенный легочный ствол и легочные артерии.
Дифференциальный диагноз при синдроме гипоплазии левых отделов сердца необходим с гипоплазией правого желудочка, единственным желудочком сердца, аномальным дренажем легочных вен, транспозицией магистральных сосудов, изолированным аортальным стенозом. Из внесердечных аномалий необходимо исключить острую дыхательную недостаточность, травму черепа, кровоизлияние в мозг.
Лечение синдрома гипоплазии левых отделов сердца
Наблюдение за новорожденными осуществляется в отделении реанимации. Для предупреждения закрытия или попытки открытия артериального протока осуществляется инфузия простагландина Е1. Необходимо проведение ИВЛ, коррекция метаболического ацидоза, введение диуретиков и инотропных препаратов.
Хирургическая коррекция гипоплазии левых отделов сердца проводится поэтапно и последовательно. Первый этап лечения – паллиативный; проводится в первые 2 недели жизни и заключается в выполнении операции Норвуда для уменьшения нагрузки на легочную артерию, и в то же время, для обеспечения кровоснабжения аорты. На втором этапе, в возрасте 3-6 месяцев ребенку выполняется операция Геми-Фонтена (или операция Гленна по наложению двухстороннего двунаправленного кава-пульмонального анастомоза). Окончательная гемодинамическая коррекция порока проводится примерно через год путем выполнения операции Фонтена (наложения тотального кавопульмонального анастомоза), позволяющей полностью разобщить круги кровообращения.
Прогноз синдрома гипоплазии левых отделов сердца
Порок является крайне неблагоприятным в отношении прогноза. В первый месяц жизни погибает около 90% детей с гипоплазией левых отделов сердца. Выживаемость после 1-го корригирующего этапа составляет 75 %, после 2-го — 95 %, после 3-го — 90 %. В целом через 5 лет после полной коррекции порока в живых остаются 70% детей.
Если гипоплазия левых отделов сердца выявляется у ребенка внутриутробно, ведение беременности и родоразрешение проводится в условиях специализированного перинатального медицинского центра. С первых дней жизни ребенок должен находиться под наблюдением неонатолога, детского кардиолога и кардиохирурга для проведения как можно более ранней коррекции порока.
Сглос синдром гипоплазии левых отделов сердца
«Синдром гипоплазии левых отделов сердца» (СГЛОС) — совокупность врожденных пороков развития ССС, характеризуемая выраженной гипоплазией или отсутствием полости ЛЖ и выраженной гипоплазией восходящей аорты в сочетанием с гипоплазией/атрезией митрального клапана. Кровообращение зависит от ПЖ, который кровоснабжает весь организм (МКК (малый круг кровообращения)и БКК (большой круг кровообращения) через ОАП (открытый артериальный проток). Необходимо наличие ДМПП для полного смешивания венозного возврата из БКК и МКК.
ПАТОФИЗИОЛОГИЯ
Внутриутробно существование порока не оказывает влияние на развитие плода, т. к. ПЖ обеспечивает системный кровоток через ОАП. Коронарная и церебральная перфузия обеспечивается ретроградно. После рождения сосудистое сопротивление МКК снижается, артериальный проток закрывается. В этом случае весь поток крови из легких направляется в гипоплазированные левые отделы сердца, которые не в состоянии обеспечить адекватную гемодинамику по БКК. Происходит снижение системного кровотока, развивается «циркуляторный шок» и метаболический ацидоз. При наличии небольшого ДМПП, не обеспечивающего адекватный лево-правый сброс и тем самым разгрузку ЛП, может развиться отек легких. Таким образом, жизнь пациента после рождения зависит от «качества» функционирования артериального протока и наличия большого ДМПП.
Прогноз при СГЛОС неблагоприятный. Практически все пациенты погибают в первые месяцы жизни при нарастающих явлениях гипоксемии и ацидоза.
А. Клинические проявления заболевания возникают вскоре после рождения:
— тахикардия, одышка, хрипы в легких, слабый периферический пульс;
-цианоз может быть не выражен, чаще пациенты имеют голубой оттенок кожи;
Б. Физикальное обследование:
— отсутствует расщепление II тона на основании сердца;
ДИАГНОСТИКА
Электрокардиография
-гипертрофия ПЖ (редко гипертрофия ЛЖ).
— резкое уменьшение объема, размеров ЛЖ (левый желудочек не участвует в формировании верхушки);
— гипоплазия или атрезия митрального клапана;
— гипоплазия восходящей аорты;
— ПЖ увеличен, резко расширен ствол ЛА;
— ДМПП с лево-правым сбросом;
— при резком сужении восходящей аорты кровь поступает в большой круг кровообращения через расширенный артериальный проток.
ЛЕЧЕНИЕ И НАБЛЮДЕНИЕ
Наблюдение и лечение пациентов с некорригированным СГЛОС
А. Показана в/в инфузия препаратов простагландина E1 с целью препятствовать закрытию артериального протока.
Б. По показаниям выполняется интубация трахей с последующей ИВЛ.
В. Коррекция метаболического ацидоза.
Г. Пациенты со СГЛОС должны быть осмотрены генетиком, офтальмологом и неврологом с целью выявления тяжелых сопутствующих аномалий, определяющих дальнейший прогноз на жизнь.
При установлении диагноза СГЛОС с наличием маленького/ рестриктивного ДМПП для увеличения объема лево-правого сброса и разгрузки ЛП проводится процедура Рашкинда. Показанием для выполнения процедуры является наличие рестриктивной коммуникации между предсердиями — градиент давления более 6 мм рт. ст.
Показания к хирургическому лечению:
— установленный диагноз СГЛОС.
Противопоказания к хирургическому лечению:
— недоношенность (срок гестации < 34 недель);
— малый вес при рождении (< 1500-1800 г);
— сочетание с другими врожденными аномалиями развития;
— выраженная регургитация на ТК;
— выраженная дисфункция ПЖ;
— ОЛС > 10 ед. или > 7 после применения вазодилататоров.
Хирургическая тактика
Заболевание манифестирует в первые несколько часов жизни, что является поводом дня дополнительного обследования и, в случае обращения в специализированное медицинское учреждение, для оперативного вмешательства. При сбалансированном кровотоке оперативное лечение показано в возрасте до 1 года при отсутствии признаков легочной гипертензии. Также у детей старше 1 месяца при несбалансированном кровотоке возможны суживание правой и левой ЛА и иссечение МПП для обеспечения адекватного смешивания крови и тренировки ПЖ.
Процедурой выбора при отсутствии возможности для трансплантации сердца является этапная гемодинамическая одножелудочковая коррекция. Гемодинамическая коррекция проводится в соответствии с принципами, описанными для атрезии трехстворчатого клапана. Вариант первого этапа коррекции — процедура Norwood.
В случае выраженной гипоплазии восходящей аорты (диаметр менее 2,5 мм) операцией выбора является трансплантация сердца.
Хирургическая техника
Хирургический доступ: срединная стернотомия. Монокавальная канюляция в ушко ПП, артериальная канюля устанавливается в ствол ЛА. Ветки ЛА обжимаются турникетами для 20 минутного охлаждения до центральной температуры 20°. Выделяется восходящая аорта. Восходящая аорта и ствол ЛА продольно вскрываются, накладывается анастомоз «бок-в-бок», ОАП резецируется, дефект в стенке неоаорты закрывается ксеноперикардиальной заплатой, дополнительно расширяющей дугу аорты. После этого возможно перемещение канюли в неоаорту. Производится поперечное отжатие неоарты с проведением кардиоплегии, системной перфузии и согревания. Ветви ЛА отсекаются от ствола ЛА, выполняется пластика дефекта стенки ЛА PTFE заплатой или ксеноперикардиальной заплатой. Иссекается МПП для формирования общего предсердия. Во время гипотермического ареста возможно проведение регионарной перфузии головного мозга, для этого предварительно накладывают анастомоз между PTFE протезом и брахиоцефальным стволом. Аортальную канюлю перемещают в PTFE протез, позднее при перемещении аортальной канюли в неоаорту протез лигируют (если предполагают использовать анастомоз Sano) или соединяют с ЛА (если используется классический МБТШ).
Источником для кровоснабжения МКК является МБТШ (модифицированный Блелок-Тауссиг шунт (анастомоз)) или шунт Сано (соединение PTFE протезом ПЖ и русла МКК). Выбор диаметра протеза осуществляется в зависимости от веса ребенка.
Второй и третий этапы гемодинамической коррекции не отличаются от таковых при диагнозе «Атрезия ТК».
Специфические осложнения хирургического лечения:
— сердечная слабость вплоть до шока;
— нарушения ритма сердца.
Послеоперационное наблюдение
Наблюдение осуществляется каждые 6-12 месяцев пожизненно. Контролируется состояние шунтов, анастомозов, функциональное состояние желудочков и ритм сердца. Медикаментозная терапия симптоматическая. В случае выполнения процедуры Фонтена ведение пациента аналогично больным с АТК.
Поделиться «Синдром гипоплазии левых отделов сердца (СГЛОС)»





